- 手机:
- 400-000-9928
- 电话:
- 020-36772040
- 邮箱:
- server@gdyulian.com
- 地址:
- 广州市白云区嘉禾望岗上胜东街46号上胜创意园I座
Kaiyun中国 官方网站——习近平总书记在致中国科学院建院70周年贺信中作出的“两加快一努力”重要指示要求
1949年,伴随着新中国的诞生,中国科学院成立。作为国家在科学技术方面的最高学术机构和全国自然科学与高新技术的综合研究与发展中心,建院以来,中国科学院时刻牢记使命,与科学共进,与祖国同行,以国家富强、人民幸福为己任,人才辈出,硕果累累,为我国科技进步、经济社会发展和国家安全做出了不可替代的重要贡献。更多简介 +
中国科学院院级科技专项体系包括战略性先导科技专项、重点部署科研专项、科技人才专项、科技合作专项、科技平台专项5类一级专项,实行分类定位、分级管理。
为方便科研人员全面快捷了解院级科技专项信息并进行项目申报等相关操作,特搭建中国科学院院级科技专项信息管理服务平台。了解科技专项更多内容,请点击进入→
中国科学技术大学(简称“中国科大”)于1958年由中国科学院创建于北京,1970年学校迁至安徽省合肥市。中国科大坚持“全院办校、所系结合”的办学方针,是一所以前沿科学和高新技术为主、兼有特色管理与人文学科的研究型大学。
中国科学院大学(简称“国科大”)始建于1978年,其前身为中国科学院研究生院,2012年经教育部批准更名为中国科学院大学。国科大实行“科教融合”的办学方针,与中国科学院直属研究机构(包括所、院、台、中心等),在管理体制、师资队伍、培养体系、科研工作等方面高度融合,是一所以研究生教育为主的独具特色的高等学校。
上海科技大学(简称“上科大”),由上海市人民政府与中国科学院共同举办、共同建设,由上海市人民政府主管,2013年经教育部正式批准。上科大致力于服务国家经济社会发展战略,培养科技创新创业人才,努力建设一所小规模、高水平、国际化的研究型、创新型大学。
在自然环境中,哺乳动物通过严格的有性生殖繁衍后代,有效地保障种群的遗传多样性。但在农业畜牧业、濒危动物保护、宠物复制、疾病模型创制和再生医学研究等诸多领域,人们往往需要获得基因组遗传物质完全一致的个体。体细胞克隆技术便是通过将体细胞核移植到去核卵母细胞中,经重编程形成全能性的胚胎,进而发育成与供体细胞核基因组完全相同的克隆动物。然而,长期以来,体细胞克隆技术因其克隆效率低下,严重制约了在实际生产和科研中的应用。如何提高体细胞克隆效率是这一领域的核心问题。
近日,中国科学院遗传与发育生物学研究所陆发隆团队和中国科学院脑科学与智能技术卓越创新中心孙强、刘真团队合作,在《先进科学》(Advanced Science)上发表了题为Efficient somatic cell nuclear transfer by overcoming both pre- and post-implantation epigenetic barriers的研究论文。该研究通过组合技术策略同时突破了体细胞克隆胚胎发育过程中着床前和着床后表观遗传障碍,实现了目前最高水平的小鼠体细胞克隆胚胎出生率,为哺乳动物高效体细胞克隆提供了一种切实可行的技术策略。
体细胞克隆胚胎具有完整的卵母细胞细胞质以及与供体细胞一致的基因组DNA序列,其发育效率低下主要源于表观遗传异常导致的基因表达紊乱。此前有研究发现,在着床前体细胞克隆胚胎中存在H3K9me3、H3K4me3和组蛋白乙酰化等多种组蛋白修饰异常,干预这些异常组蛋白修饰可有效改善胚胎的着床前发育。进一步,有研究发现小鼠体细胞克隆胚胎中非典型基因印记缺失;进而通过在供体细胞中多基因杂合敲除以模拟主要非典型印记基因的印记表达状态,证明修复非典型基因印记能有效改善体细胞克隆胚胎的着床后发育。然而,之前尚未有研究能同时解决着床前与着床后的表观遗传障碍,且现有用于修复着床后非典型印记的方法技术难度极大。
此项研究中,研究团队通过对体细胞克隆胚胎施以组蛋白去乙酰化酶抑制剂曲古抑菌素A (TSA)处理,同时向胚胎中注射编码H3K9me3去甲基化酶Kdm4d和H3K4me3去甲基化酶Kdm5b的mRNA干预异常组蛋白修饰,有效解决了体细胞克隆胚胎着床前发育表观遗传障碍。同时,利用四倍体补偿技术替换了克隆胚胎的滋养层细胞,有效处理了克隆胚胎胎盘组织中非典型基因印记缺失问题,从而解决了体细胞克隆胚胎着床后发育表观遗传障碍。通过这种组合体细胞克隆胚胎表观遗传障碍干预技术策略,实现了体细胞克隆小鼠移植胚胎约30%的出生率。
该研究首次在单一体细胞克隆胚胎内同时克服了着床前和着床后发育的主要表观遗传障碍,且无需对供体细胞进行额外的遗传修饰,极大提高了哺乳动物体细胞克隆的整体效率,有望为今后大型哺乳动物通过体细胞克隆进行成本可控的高效繁殖提供新技术策略。
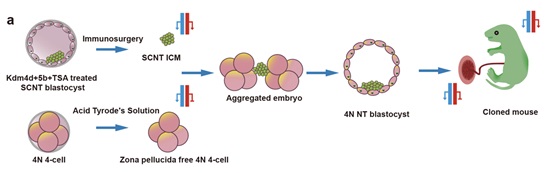
在自然环境中,哺乳动物通过严格的有性生殖繁衍后代,有效地保障种群的遗传多样性。但在农业畜牧业、濒危动物保护、宠物复制、疾病模型创制和再生医学研究等诸多领域,人们往往需要获得基因组遗传物质完全一致的个体。体细胞克隆技术便是通过将体细胞核移植到去核卵母细胞中,经重编程形成全能性的胚胎,进而发育成与供体细胞核基因组完全相同的克隆动物。然而,长期以来,体细胞克隆技术因其克隆效率低下,严重制约了在实际生产和科研中的应用。如何提高体细胞克隆效率是这一领域的核心问题。近日,中国科学院遗传与发育生物学研究所陆发隆团队和中国科学院脑科学与智能技术卓越创新中心孙强、刘真团队合作,在《先进科学》(Advanced Science)上发表了题为Efficient somatic cell nuclear transfer by overcoming both pre- and post-implantation epigenetic barriers的研究论文。该研究通过组合技术策略同时突破了体细胞克隆胚胎发育过程中着床前和着床后表观遗传障碍,实现了目前最高水平的小鼠体细胞克隆胚胎出生率,为哺乳动物高效体细胞克隆提供了一种切实可行的技术策略。体细胞克隆胚胎具有完整的卵母细胞细胞质以及与供体细胞一致的基因组DNA序列,其发育效率低下主要源于表观遗传异常导致的基因表达紊乱。此前有研究发现,在着床前体细胞克隆胚胎中存在H3K9me3、H3K4me3和组蛋白乙酰化等多种组蛋白修饰异常,干预这些异常组蛋白修饰可有效改善胚胎的着床前发育。进一步,有研究发现小鼠体细胞克隆胚胎中非典型基因印记缺失;进而通过在供体细胞中多基因杂合敲除以模拟主要非典型印记基因的印记表达状态,证明修复非典型基因印记能有效改善体细胞克隆胚胎的着床后发育。然而,之前尚未有研究能同时解决着床前与着床后的表观遗传障碍,且现有用于修复着床后非典型印记的方法技术难度极大。此项研究中,研究团队通过对体细胞克隆胚胎施以组蛋白去乙酰化酶抑制剂曲古抑菌素A (TSA)处理,同时向胚胎中注射编码H3K9me3去甲基化酶Kdm4d和H3K4me3去甲基化酶Kdm5b的mRNA干预异常组蛋白修饰,有效解决了体细胞克隆胚胎着床前发育表观遗传障碍。同时,利用四倍体补偿技术替换了克隆胚胎的滋养层细胞,有效处理了克隆胚胎胎盘组织中非典型基因印记缺失问题,从而解决了体细胞克隆胚胎着床后发育表观遗传障碍。通过这种组合体细胞克隆胚胎表观遗传障碍干预技术策略,实现了体细胞克隆小鼠移植胚胎约30%的出生率。该研究首次在单一体细胞克隆胚胎内同时克服了着床前和着床后发育的主要表观遗传障碍,且无需对供体细胞进行额外的遗传修饰,极大提高了哺乳动物体细胞克隆的整体效率,有望为今后大型哺乳动物通过体细胞克隆进行成本可控的高效繁殖提供新技术策略。该研究得到科技部、中国科学院、国家自然科学基金委等的支持。研究方法示意图














